研究背景:
多氟烷基磷酸酯(PAPs)广泛应用于食品包装、个人护理品等,被作为传统全氟和多氟烷基物质(PFASs)的替代品大量使用,对环境和人体健康带来不可忽视的负担。
PAPs 在环境介质(如水体、沉积物、灰尘)和人体样品(血液、母乳、尿液)中普遍存在,其中 8:2 二磷酸酯(8:2 diPAP)是检测频率最高的种类之一,具有环境持久性和肝脏富集性。既往研究表明 8:2 diPAP 可引起内分泌干扰、氧化损伤和生殖毒性,但其在哺乳动物中的肝毒性作用及免疫学机制尚不清楚;巨噬细胞极化(M1/M2)在肝脏炎症与疾病进展中扮演重要角色,但尚无研究系统探讨 8:2 diPAP 是否通过该机制诱导肝损伤。
研究内容:
1.建立小鼠灌胃暴露模型,剂量分别为 0.5、5 和 50 mg/kg,暴露时间为 28 天。
2.通过血清学指标(T-Bil、ALB、ALT、AST)、肝组织学观察(HE 染色)评估肝损伤情况。
3.检测肝脏中炎症因子(Il1b, Il6, Tnfa)、M1/M2 型巨噬细胞标志物表达,并结合免疫荧光分析巨噬细胞极化情况。
4.利用 GO/KEGG 富集分析、分子对接及蛋白水平检测,探讨 8:2 diPAP 与 JAK2/STAT3 信号通路的关系。
5.分析 Jak2、Stat3、p-Stat3、Socs3 蛋白表达变化,揭示分子机制。
研究结论:
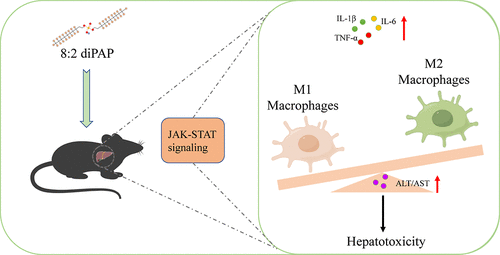
本研究开发了一种小鼠模型来评估 8:2 多氟烷基磷酸二酯(8:2 diPAP)的肝毒性作用和机制。暴露于剂量为 0.5、5和50 mg/kg 的 8:2 diPAP 会导致肝细胞损伤和血清总胆红素水平升高。50 mg/kg 8:2 diPAP组白蛋白、丙氨酸转氨酶和天冬氨酸转氨酶显著升高。在8:2 diPAP暴露下,肝脏中M1型巨噬细胞标志物的表达和M1巨噬细胞的比例显著增加。Janus激酶/信号转导和转录激活因子(JAK/STAT)信号传导在8:2 diPAP暴露下显著富集。分子对接显示8:2 diPAP-JAK2 直接结合,Western blot分析显示暴露小鼠肝脏 Jak2 表达降低。暴露肝脏中Stat3磷酸化增加和Socs3表达降低表明,8:2 diPAP通过抑制Socs3激活Stat3通路,从而促进M1巨噬细胞极化。研究结果表明,8:2 diPAP 暴露通过驱动小鼠 M1 巨噬细胞极化来诱导肝损伤。
研究意义:
本研究首次在哺乳动物中证实 8:2 diPAP 通过 Socs3/Jak2/Stat3 信号通路介导的 M1 巨噬细胞极化诱导肝损伤。研究为 PAPs 的健康风险评估提供了新的证据,也表明需更新PAPs的相关环境和健康风险管控标准。
原文链接:https://pubs.acs.org/doi/10.1021/acs.est.5c06681
